Cacbon có hai đồng vị \(^{12}_6C\) và \(^{13}_6C\) và có nguyên tử khối là 12,011. Tình % các đồng vị C

Những câu hỏi liên quan
Cacbon tự nhiên là hỗn hợp của hai đồng vị
C
12
và
C
12
, trong đó đồng vị
C
12
chiếm 98,9%.Biết rằng đồng vị
C
12
có nguyên tử khối bằng 13,0034, đồng vị
C...
Đọc tiếp
Cacbon tự nhiên là hỗn hợp của hai đồng vị C 12 và C 12 , trong đó đồng vị C 12 chiếm 98,9%.
Biết rằng đồng vị C 12 có nguyên tử khối bằng 13,0034, đồng vị C 12 có nguyên tử khối bằng 12, nguyên tử khối trung bình của cacbon là
A. 12,150. B. 12,011.
C. 12,512. D. 12,250.
Trong tự nhiên cacbon có 2 đồng vị bền 12 6 C và 13 6 C . Nguyên tử khối trung bình của nguyên tố cacbon là 12,011.
- Tính thành phần phần trăm số nguyên tử của mỗi đồng vị cacbon.
- Tính thành phần phần trăm khối lượng của 12C có trong K2CO3 (với K là đồng vị 39 19 K ; O là đồng vị 16 8 O ).
Trong tự nhiên cacbon có 2 đồng vị bền 12 6 C và 13 6 C . Nguyên tử khối trung bình của nguyên tố cacbon là 12,011. - Tính thành phần phần trăm số nguyên tử của mỗi đồng vị cacbon. - Tính thành phần phần trăm khối lượng của 12C có trong C2H6 (với H là đồng vị 1 1H )
Trong tự nhiên cacbon có 2 đồng vị bền 12 6 C và 13 6 C . Nguyên tử khối trung bình của nguyên tố cacbon là 12,011. - Tính thành phần phần trăm số nguyên tử của mỗi đồng vị cacbon. - Tính thành phần phần trăm khối lượng của 12C có trong C2H6 (với H là đồng vị 1 1H )
Bài 1. Tính thành phần phần % các đồng vị của cacbon. Biết cacbon trong tự nhiên tồn tại hai đồng vị bền là 12C và 13C và có nguyên tử trung bình là 12,011.Bài 2. Nguyên tử khối trung bình của Ag là 107,87, trong tự nhiên bạc có hai đồng vị là 107Ag và 109Ag. Xác định % số nguyên tử của mỗi đồng vị.Tính % theo khối lượng của đồng vị 109Ag trong AgNO3 (lấy nguyê tử khối tb N 14; O 16)
Đọc tiếp
Bài 1. Tính thành phần phần % các đồng vị của cacbon. Biết cacbon trong tự nhiên tồn tại hai đồng vị bền là 12C và 13C và có nguyên tử trung bình là 12,011.
Bài 2. Nguyên tử khối trung bình của Ag là 107,87, trong tự nhiên bạc có hai đồng vị là 107Ag và 109Ag. Xác định % số nguyên tử của mỗi đồng vị.
Tính % theo khối lượng của đồng vị 109Ag trong AgNO3 (lấy nguyê tử khối tb N = 14; O = 16)
Gọi x,y lần lượt là phần trăm đồng vị của 12C và 13C
Ta có: \(\left\{{}\begin{matrix}x+y=100\\12.0,01x+13.0,01y=12,011\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=100-y\\0,12.\left(100-y\right)+0,13.y=12,011\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}x=98,9\%\\y=1,1\%\end{matrix}\right.\)
Đúng 5
Bình luận (0)
Trong tự nhiên cacbon có 2 đồng vị bền là C 6 12 và C 6 13 . Nguyên tử khối trung bình của cacbon là 12,011. Phần trăm số nguyên tử của 2 đồng vị trên lần lượt là
A. 98,9% và 1,1%.
B. 49,5% và 51,5%.
C. 99,8% và 0,2%.
D. 75% và 25%.
Chọn A
Gọi % số nguyên tử của đồng vị C 6 13 là x %, thì % số nguyên tử của đồng vị C là 100 – x (%).
Ta có
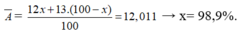
Đúng 0
Bình luận (0)
Câu 3: Carbon có 2 đồng vị dfrac{12}{6} C, dfrac{13}{6} C và có nguyên tử khối là 12,011. Tính thành phần % về số mol của mỗi loại đồng vị .
Đọc tiếp
Câu 3: Carbon có 2 đồng vị \(\dfrac{12}{6}\) C, \(\dfrac{13}{6}\) C và có nguyên tử khối là 12,011. Tính thành phần % về số mol của mỗi loại đồng vị .
Gọi: %12C = x%
⇒ %13C = (100 - x) %
\(\Rightarrow12.x\%+13.\left(100-x\right)\%=12,011\)
⇒ x = 98,9% = %12C
⇒ %13C = 100 - 98,9 = 1,1%
Đúng 1
Bình luận (0)
Nguyên tố cacbon có hai đồng vị: chiếm 98,89% và chiếm 1,11% Nguyên tử khối trung bình của cacbon là: a) 12,500. b) 12,011. c) 12,022. d) 12,055. Chọn đáp án đúng.
Đọc tiếp
Nguyên tố cacbon có hai đồng vị: 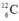 chiếm 98,89% và
chiếm 98,89% và 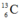 chiếm 1,11%
chiếm 1,11%
Nguyên tử khối trung bình của cacbon là:
a) 12,500.
b) 12,011.
c) 12,022.
d) 12,055.
Chọn đáp án đúng.
Trong tự nhiên cacbon có 2 đồng vị bền là C 6 12 và C 6 13 . Nguyên tử khối trung bình của cacbon là 12,011. Phần trăm của 2 đồng vị trên lần lượt là
A. 98,9% và 1,1%.
B. 49,5% và 51,5%.
C. 99,8% và 0,2%.
D. 75% và 25%.
Chọn A
Gọi % của đồng vị 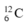 là x, thì % của đồng vị
là x, thì % của đồng vị 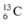 là 100 - x
là 100 - x
Ta có
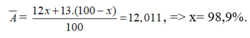 .
.
Đúng 0
Bình luận (0)